Cơ Quan Quản Lý Thực Phẩm và Dược Phẩm Hoa Kỳ (FDA) đã phê duyệt một số thuốc điều trị Covid -19 và cấp phép sử dụng khẩn cấp trong các trường hợp khẩn cấp của bệnh hô hấp cấp tính này. Ngoài ra, một số liệu pháp khác đang trong giai đoạn thử nghiệm lâm sàng để đánh giá tính an toàn và hiệu quả trong việc chống lại Covid-19.
Tổng quát về bệnh Covid-19
Bệnh Covid-19 là bệnh do một loại coronavirus gây ra, hiện được gọi là SARS-CoV-2 gây hội chứng hô hấp cấp tính nghiêm trọng, được phát hiện đầu tiên vào ngày 31 tháng 12 năm 2019 ở thành phố Vũ Hán, tỉnh Hồ Bắc, Trung Quốc. Vào ngày 30 tháng 1 năm 2020, WHO tuyên bố đợt bùng phát Covid-19 là tình trạng khẩn cấp về sức khỏe toàn cầu. Vào ngày 11 tháng 3 năm 2020, WHO tuyên bố Covid-19 là đại dịch toàn cầu.

Bệnh Covid-19 gây hội chứng hô hấp cấp tính nghiêm trọng
Trong thời kỳ đại dịch, các chương trình do FDA thiết lập cho phép các bác sĩ tiếp cận với các liệu pháp điều trị Covid 19 là rất cần thiết. Các chương trình tiếp cận mở rộng (EA) và cấp phép sử dụng khẩn cấp (EUA) cho phép triển khai nhanh chóng các liệu pháp điều trị tiềm năng và các liệu pháp điều trị với bằng chứng mới nhất.
1. Thuốc điều trị Covid cấp phép sử dụng khẩn cấp (EUA)
Thuốc kháng virus Remdesivir Veklury) và vacxin Covid-19 mRNA (Comirnaty) đã được FDA phê duyệt hoàn toàn. Tuy nhiên, các chỉ định và đối tượng sử dụng cho từng liệu pháp này vẫn nằm trong EUA của họ.
Các tờ thông tin của EUA dành cho các bác sĩ lâm sàng cung cấp thông tin chi tiết về các các thuốc, sinh phẩm và vacxin được EUA ban hành như một liệu pháp điều trị hoặc phòng ngừa Covid-19.

Covid-19 EUAs
2. Thuốc kháng virus
* Remdesivir
Remdesivir được FDA chấp thuận hoàn toàn để điều trị Covid-19 ở người lớn và bệnh nhi từ 12 tuổi trở lên (trên 40kg cân nặng). Remdesivir điều trị Covid 19 có mức độ bệnh từ nhẹ đến trung bình, có nhiều nguy cơ tiến triển thành Covid 19 nghiêm trọng, bao gồm cả nhập viện hoặc tử vong.
Remdesivir cấp phép sử dụng khẩn cấp điều trị Covid-19 ở bệnh nhi nhập viện có cân nặng từ 3,5kg đến dưới 40kg hoặc bệnh nhi nhập viện dưới 12 tuổi có cân nặng ít nhất 3,5kg. Ngoài ra, Remdesivir được chỉ định điều trị cho bệnh nhân ngoại trú mắc Covid-19 mức độ nhẹ đến trung bình, những người có nguy cơ cao tiến triển thành Covid-19 nghiêm trọng, bao gồm cả nhập viện hoặc tử vong.
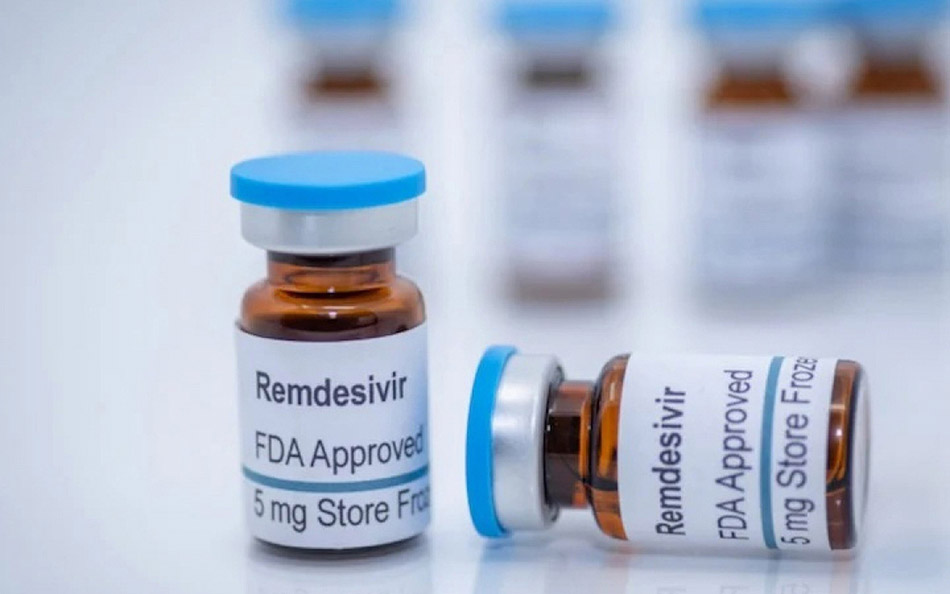
Thuốc Remdesivir
* Nirmatrelvir / Ritonavir
Nirmatrelvir / Ritonavir đã được ban hành và được cấp phép sử dụng khẩn cấp điều trị coronavirus từ nhẹ đến trung bình ở người lớn và bệnh nhi ngoại trú (từ 12 tuổi trở lên và nặng ít nhất 40kg, có nguy cơ tiến triển thành Covid 19 nghiêm trọng, bao gồm cả nhập viện và tử vong.
* Molnupiravir
Molnupiravir được ban hành và cấp phép sử dụng khẩn cấp để điều trị Covid-19 ở bệnh nhân ngoại trú người lớn, có nguy cơ cao tiến triển thành Covid-19 nặng, bao gồm cả nhập viện và tử vong.
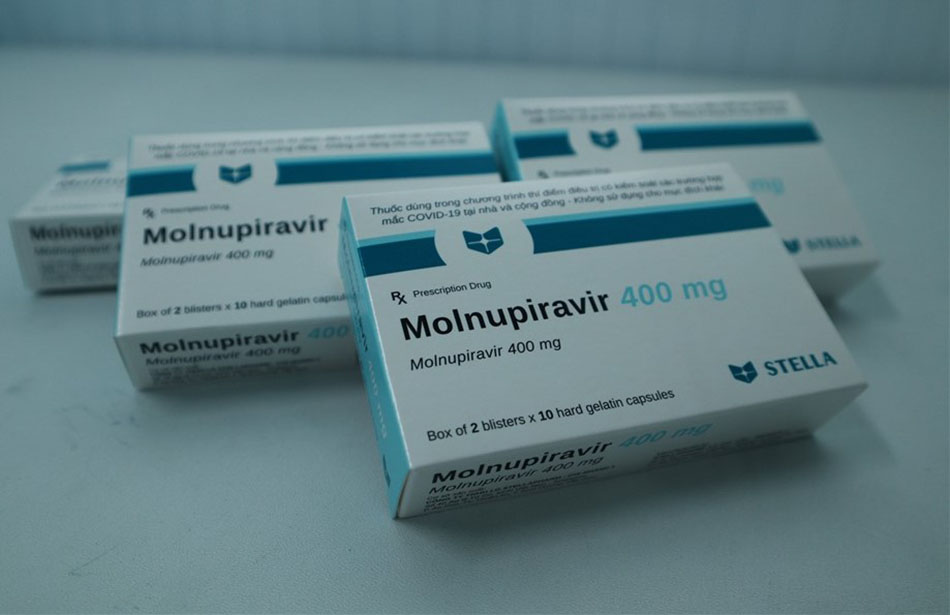
Thuốc Molnupiravir
* Tocilizumab
Tocilizumab được cấp phép sử dụng khẩn cấp để điều trị Covid-19 cho người lớn và bệnh nhi từ 2 tuổi trở lên nằm viện và đang được điều trị bằng corticosteroid toàn thân cần được bổ sung oxy, thở máy không xâm lấn hoặc xâm lấn hoặc oxy qua màng ngoài cơ thể (ECMO).
* Baricitinib
Baricitinib được cấp phép sử dụng khẩn cấp điều trị bệnh Covid-19 nghi ngờ hoặc đã được xác nhận trong phòng thí nghiệm ở bệnh nhân từ 2 tuổi trở lên, những người cần bổ sung oxy, thở máy xâm nhập hoặc oxy qua màng ngoài cơ thể (ECMO).

Baricitinib điều trị Covid-19
* Kháng thể đơn dòng
Kháng thể đơn dòng được cấp phép điều trị khẩn cấp cho các bệnh nhân ngoại trú (Ví dụ: Sotrovimab, Casirivimab/Imdevimab, Bamlanivimab/Etesevimab) từ 12 tuổi trở lên (cân nặng ít nhất 40kg) mắc Covid-19 và có nguy cơ cao thành Covid-19 nghiêm trọng hoặc nhập viện.
Dự phòng sau phơi nhiễm: Casirivimab/Imdevimab và Bamlanivimab/Etesevimab.
Dự phòng trước phơi nhiễm: Tixagevimab/Cilgavimab được sử dụng điều trị dự phòng trước phơi nhiễm cho những bệnh nhân suy giảm miễn dịch mức độ trung bình đến nặng, do tình trạng y tế hoặc thuốc/điều trị, không đáp ứng miễn dịch hoặc có tiền sử phản ứng có hại nghiêm trọng đối với vacxin Covid-19.

Thuốc kháng thể đơn dòng
* Huyết tương hồi phục
Huyết tương hồi phục điều trị Covid 19 trong trường hợp khẩn cấp được EUA ban hành vào tháng 8 năm 2020. Tuy nhiên, dữ liệu từ một nghiên cứu công bố vào năm 2021 cho thấy, huyết tương hồi phục không ngăn ngừa được tình trạng bệnh trở nên trầm trọng hơn ở những bệnh nhân có nguy cơ cao được đưa vào khoa cấp cứu trong tuần đầu tiên khi bệnh nhân có triệu chứng.
Các nghiên cứu bổ sung đang được tiến hành để xác định xem liệu lợi ích của huyết tương hồi phục có thể được quan sát thấy ở nhóm đối tượng khác hay không.

Huyết tương hồi phục
* Vacxin
Vacxin đầu tiên được FDA chấp thuận đầy đủ là mRNA (Comirnaty, Pfizer) vào tháng 8 năm 2021. FDA cũng cấp phép sử dụng khẩn cấp cho 2 vacxin khác kể từ tháng 12 năm 2020 là mRNA-1273 (Moderna) và vacxin vectơ virus Ad26.COV2.S của Janssen (Johnson & Johnson).
Tài liệu tham khảo
1. Tác giả: Bác sĩ Nguyễn Lân Hiếu, Nguyễn Trang Thúy, Nguyễn Văn Hiếu, Nguyễn Phương Mai, Vũ Việt Hà. Ngày đăng: 19 tháng 02 năm 2022. Thuốc và các chế phẩm điều trị Covid-19. Nhathuocngocanh.com. Ngày truy cập: 20/02/2022.
2. Tác giả: Dược sĩ Trung Tâm Thuốc Cetral Pharmacy (Ngày đăng: ngày 6 tháng 11 năm 2021). Molnupiravir. Trung Tâm Thuốc Cetral Pharmacy. Truy cập ngày 20 tháng 2 năm 2022.
3. Tác giả: Scott J Bergman, PharmD (Ngày đăng: ngày 9 tháng 2 năm 2022). COVID-19 Treatment: Investigational Drugs and Other Therapies, Medscape. Truy cập ngày 20 tháng 2 năm 2022.
4.Tác giả: Bác sĩ Đồng Phú Khiêm, Nguyễn Thị Ngọc, Nguyễn Phương Mai, Nguyễn Lân Hiếu. Ngày đăng: 17 tháng 02 năm 2022. Điều trị bệnh nhân COVID-19 nhập viện. Nhathuocngocanh.com. Truy cập ngày 20 tháng 2 năm 2022.
Dược sỹ Lưu Anh (Cộng tác viên)